國(guó)務(wù)院常務(wù)會(huì)決定再壓減工業(yè)產(chǎn)品生產(chǎn)許可證三分之一以上并簡(jiǎn)化審批,為市場(chǎng)主體減負(fù)。在國(guó)新辦21日召開(kāi)的國(guó)務(wù)院政策例行吹風(fēng)會(huì)上,國(guó)家市場(chǎng)監(jiān)管總局副局長(zhǎng)田世宏進(jìn)行了解讀。
利昂醫(yī)療的總工程師介紹,這次改革主要體現(xiàn)在4個(gè)方面:
一是大幅壓減許可證管理目錄。改革取消了14類產(chǎn)品,推動(dòng)其中部分產(chǎn)品轉(zhuǎn)認(rèn)證,下放了4類產(chǎn)品由省級(jí)部門實(shí)施。
二是推動(dòng)“一企一證”改革。對(duì)繼續(xù)實(shí)施生產(chǎn)許可證管理的產(chǎn)品,按照“一企一證”的要求發(fā)證。凡是跨類別生產(chǎn)的企業(yè),新申請(qǐng)?jiān)S可證時(shí),一并審查頒發(fā)一張證書(shū);換發(fā)許可證時(shí),將多種類別產(chǎn)品的許可合并到一張證書(shū)上。
三是著力調(diào)整產(chǎn)品檢驗(yàn)和現(xiàn)場(chǎng)審查兩個(gè)關(guān)鍵環(huán)節(jié)。在全國(guó)范圍內(nèi),將發(fā)證前產(chǎn)品檢驗(yàn),改為由企業(yè)在申請(qǐng)時(shí)提交符合要求的產(chǎn)品檢驗(yàn)合格報(bào)告,這樣也是節(jié)省時(shí)間,保證快速地發(fā)證書(shū)。除危險(xiǎn)化學(xué)品外,對(duì)省級(jí)部門管理的產(chǎn)品實(shí)行后置現(xiàn)場(chǎng)審查,企業(yè)提交申請(qǐng)和產(chǎn)品檢驗(yàn)報(bào)告,并作出保障質(zhì)量承諾后,經(jīng)形式審查合格即可取證,之后在規(guī)定時(shí)間內(nèi)接受現(xiàn)場(chǎng)審查。
四是加大證后監(jiān)管力度。對(duì)通過(guò)簡(jiǎn)化程序取證的企業(yè),加強(qiáng)企業(yè)“一單一書(shū)一照一報(bào)告”(即申請(qǐng)?jiān)S可證需提交的申請(qǐng)單、承諾書(shū)、營(yíng)業(yè)執(zhí)照和產(chǎn)品檢驗(yàn)合格報(bào)告)承諾公示,加強(qiáng)后置現(xiàn)場(chǎng)審查;對(duì)虛假承諾、不符合要求的,一律撤銷生產(chǎn)許可證;加強(qiáng)信用監(jiān)管,運(yùn)用信用激勵(lì)和約束手段,督促企業(yè)落實(shí)質(zhì)量主體責(zé)任。
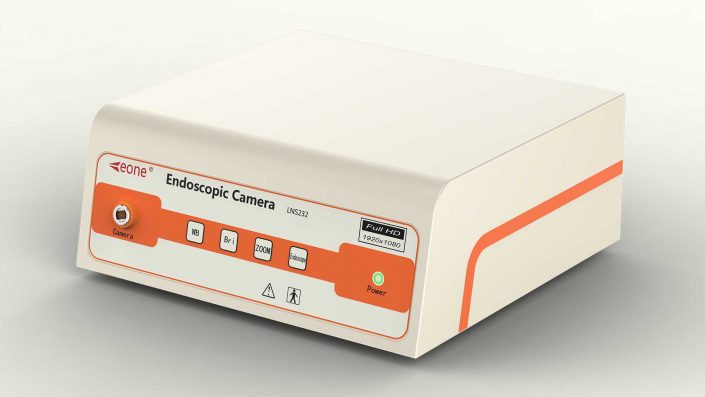
這點(diǎn)在醫(yī)療行業(yè)也是如此,加大監(jiān)管力度,提高創(chuàng)新醫(yī)療器械的生產(chǎn),多一些如南京利昂醫(yī)療的內(nèi)窺鏡攝像機(jī)等的好的產(chǎn)品!
深化工業(yè)產(chǎn)品生產(chǎn)許可證制度改革,是推進(jìn)放管服改革的重大措施之一。
近年來(lái),為了進(jìn)一步優(yōu)化營(yíng)商環(huán)境,適應(yīng)市場(chǎng)經(jīng)濟(jì)發(fā)展的需要,對(duì)生產(chǎn)許可證制度做了大量調(diào)整。在前期改革基礎(chǔ)上,著力壓減生產(chǎn)許可證管理目錄、著力簡(jiǎn)化審批程序,營(yíng)造更加公開(kāi)透明便利的準(zhǔn)入環(huán)境,進(jìn)一步釋放市場(chǎng)和社會(huì)創(chuàng)造力。